気体 の 状態 変化
熱学 (気体の状態変化) ホーム メニュー 熱と仕事 気体の法則 気体分子運動論 内部エネルギー 気体の状態変化 不可逆変化 いろいろな状態変化 (各状態変化は右図の①~④) 物質量 n molの場合 ① 定積変化 ( V 一定) 体積が一定だから⊿ V =0, Q = nC V ⊿ T.

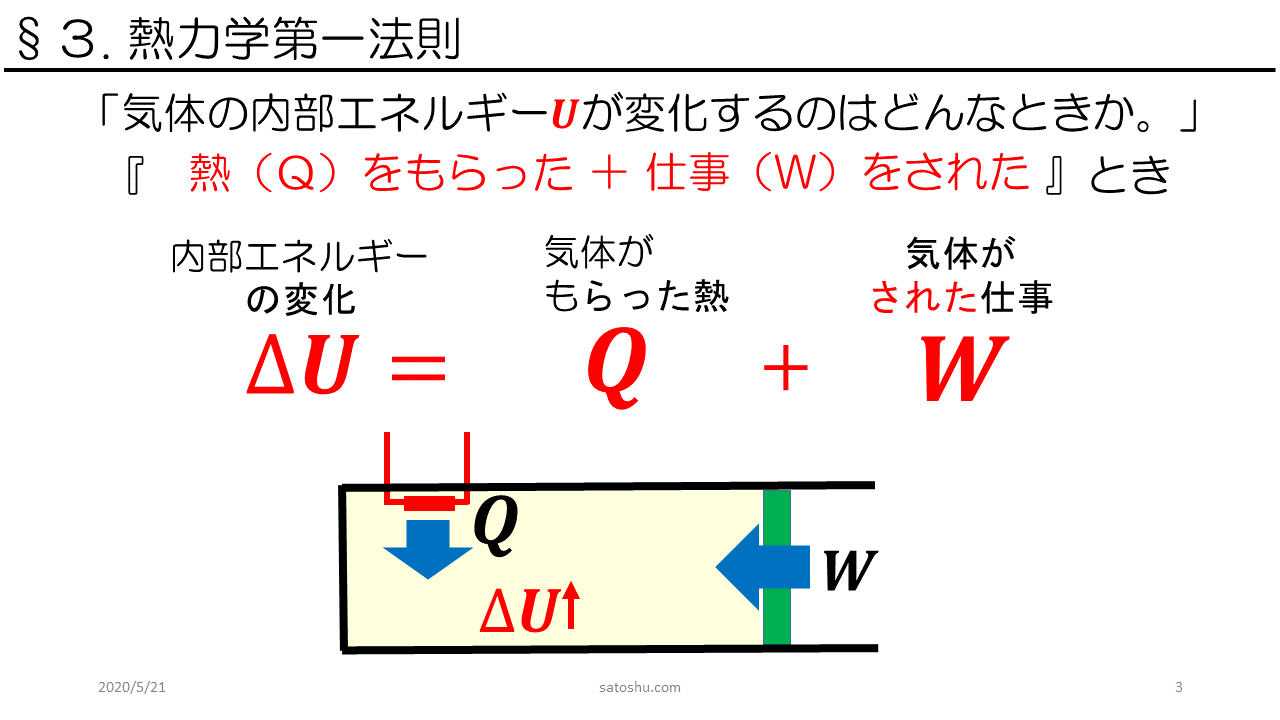
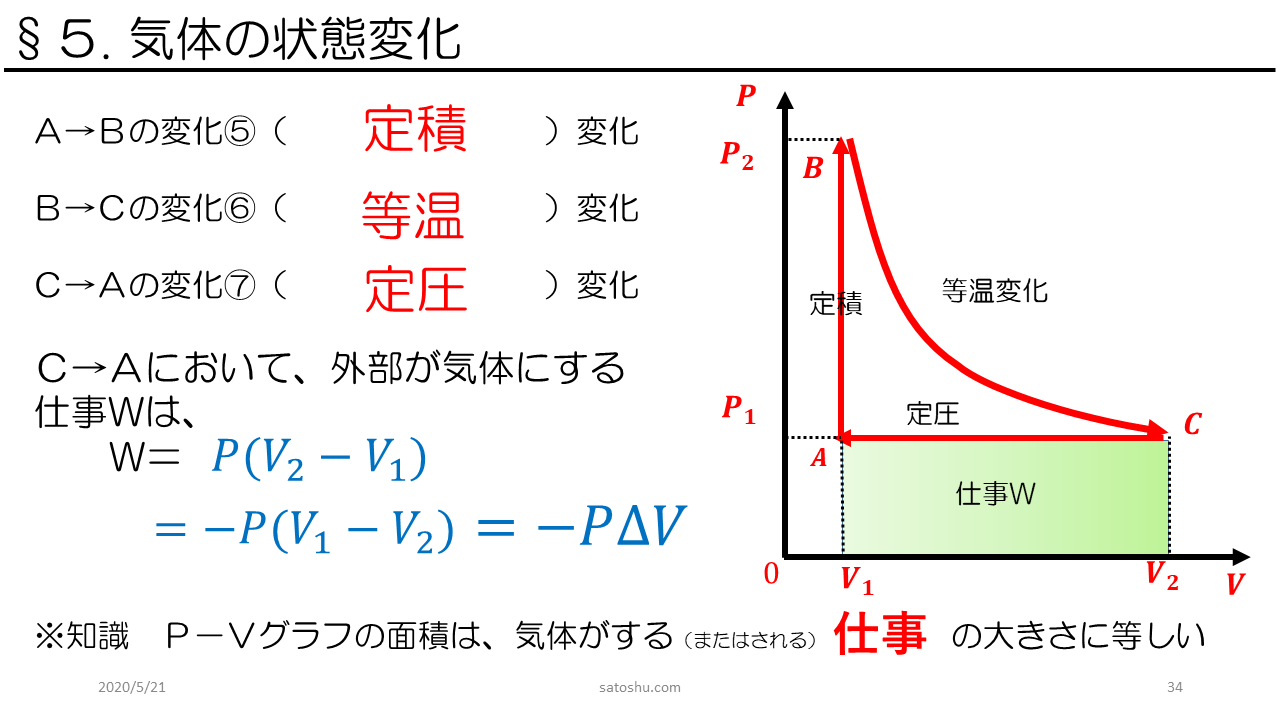
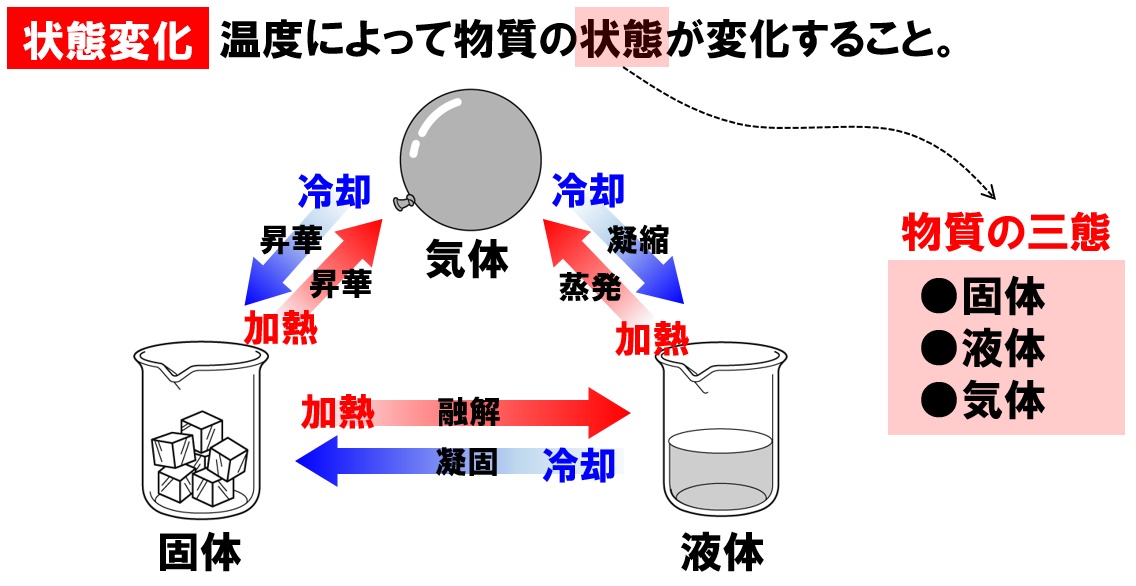
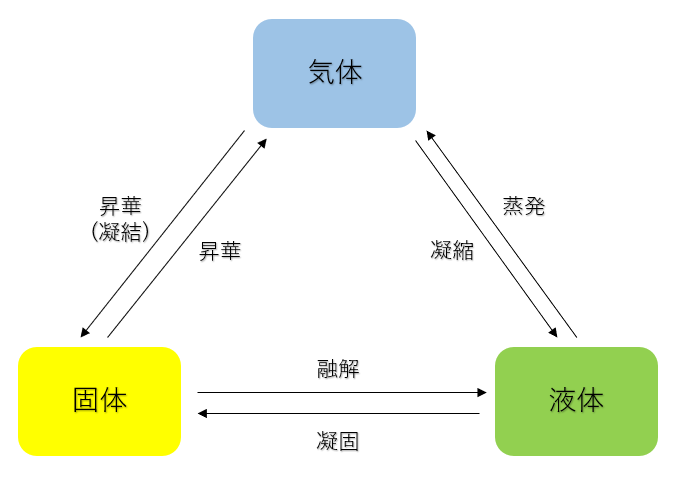
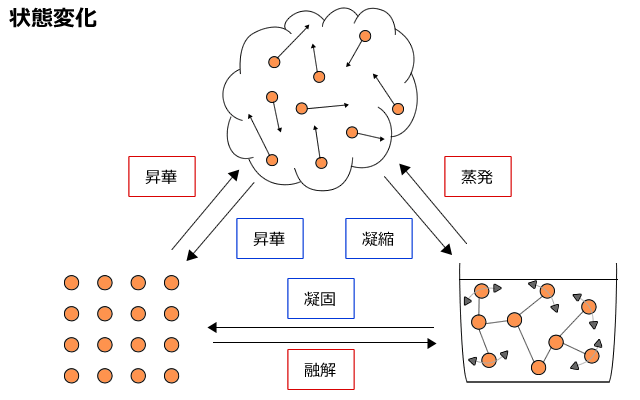
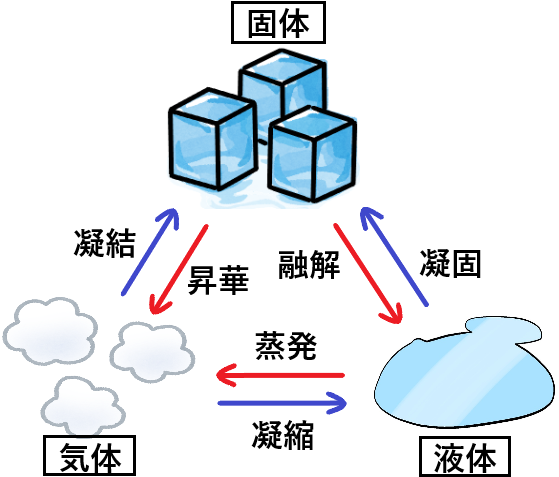
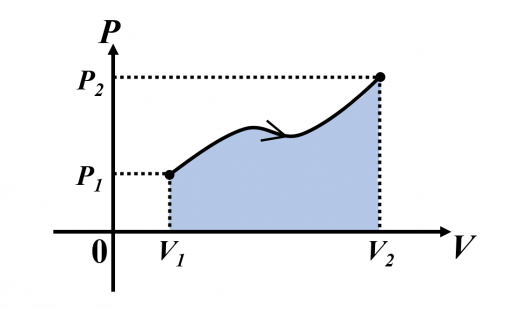
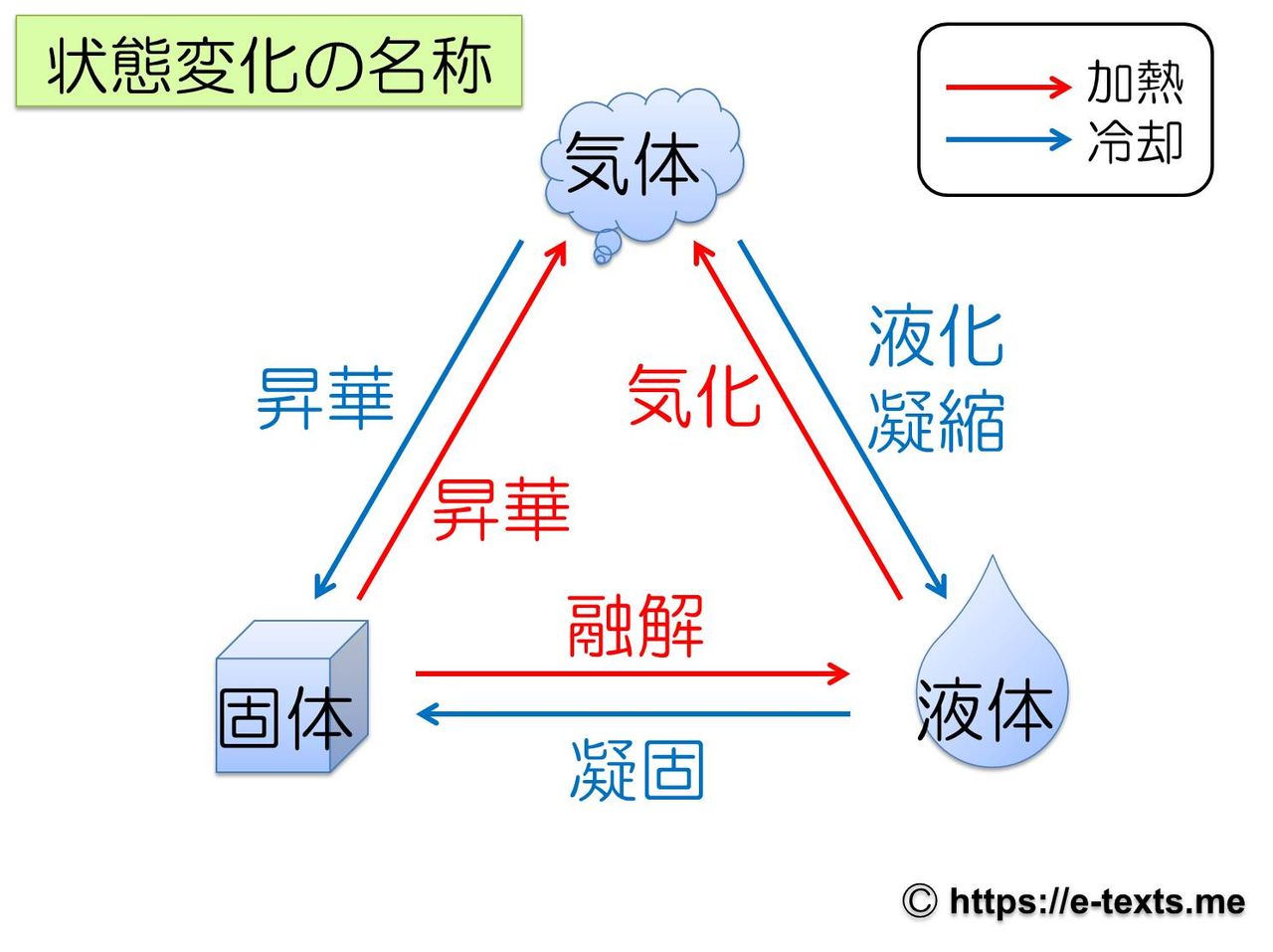
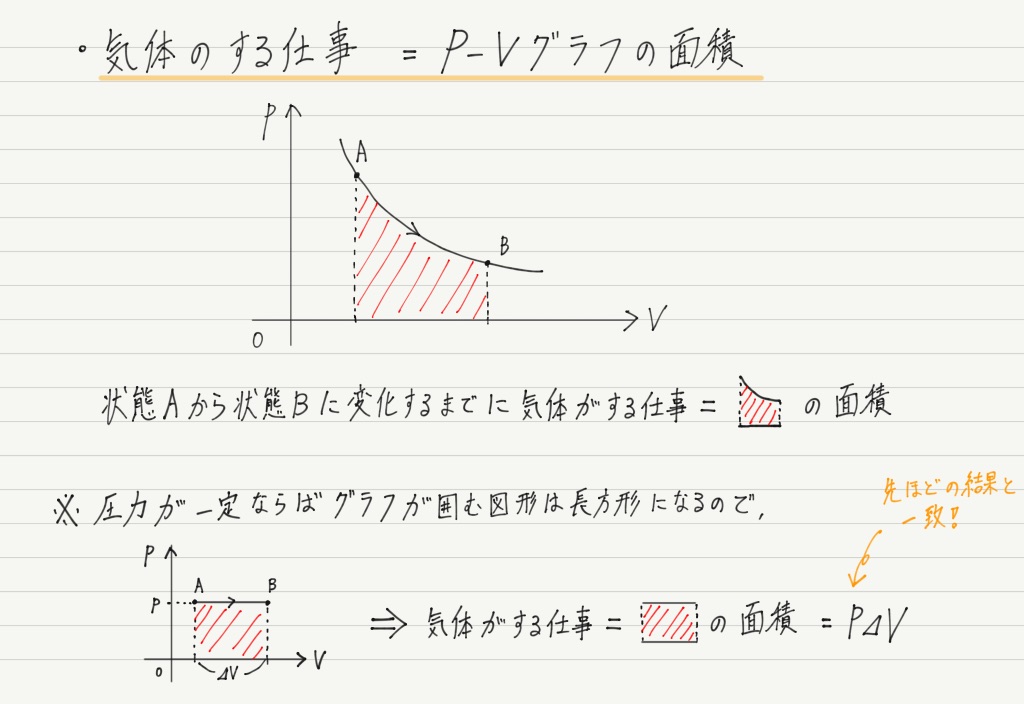
気体 の 状態 変化. 気体の状態変化を表す便利なグラフとして, 縦軸に圧力 P , 横軸に体積 V をとった P V グラフ が知られている P V グラフの意味を明確にするために, 系が外部に対して行った仕事 W の計算方法について考える 力学の章で取り扱ったように, 仕事とは力と微小変位の積の総和 であり 圧力と体積の微小変化の積の総和と同義である したがって, 気体が外部にする仕事は力 (もしくは圧力)の加えられて. 状態変化とは 物質はあたためたり、冷やしたりすることで 固体、液体、気体 と状態が変化する。 このように 温度によって物質の状態が変わることを状態変化という。 凝縮 凝固 融解 蒸発 昇華 昇華 凝縮 凝固 融解 蒸発 昇華 昇華 固体 液体 気体 固体を加熱すると液体になり、液体を加熱すると気体になる。 また気体を冷やすと液体に、液体を冷やすと固体になる。 物質によっては固体から気体、気. 体積が一定に保たれる条件で起こる変化。 4つの物理過程 (理想気体、可逆過程、 が一定の場合) なお、次の式はどの過程でも成り立ちます。 上の表の数式は全て下の6つの式から導かれています。 気体をある状態から別の状態へ変化させるには無数の経路がありますが、 通常、上記の 4 つの過程 (等温、断熱、定圧、定容) の組み合わせで考えます 2) 。 例えば 1 mol の理想気体が、状態 1 (400 K, 2.
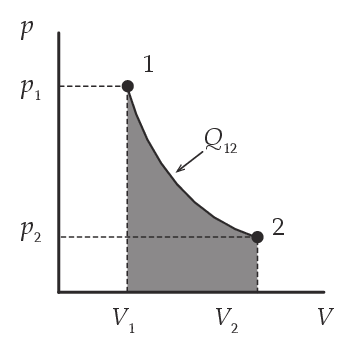
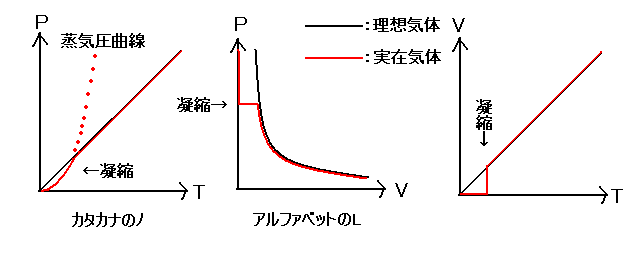
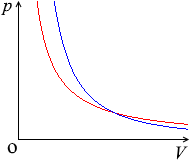
一方、実際に存在する酸素o 2 や二酸化炭素co 2 などの気体は 実在気体 と呼ばれ、分子に体積があり、分子間力が働いている。 実在気体において、気体の状態方程式は成り立たない。 理想気体と実在気体の比較を表にまとめると次のようになる。. 固体が液体になったり、気体が液体になったりする変化は、私たちのまわりで頻繁に起きていますよね。 このように、ある物質が固体・液体・気体の間を変化することを、 状態変化 といいます。 この状態変化こそが、今回のメインテーマなのです。 状態変化は、融解・蒸発・凝縮・凝固・昇華 状態変化の名前については、以前に学習したことがあると思います。 固体⇒液体: 融解 液体⇒気体: 蒸. 気体の状態方程式 PV=nRT ※P=圧力 (Pa) n=物質量 (mol) V=体積 (L) R=気体定数 T=温度 (K) P o int!.
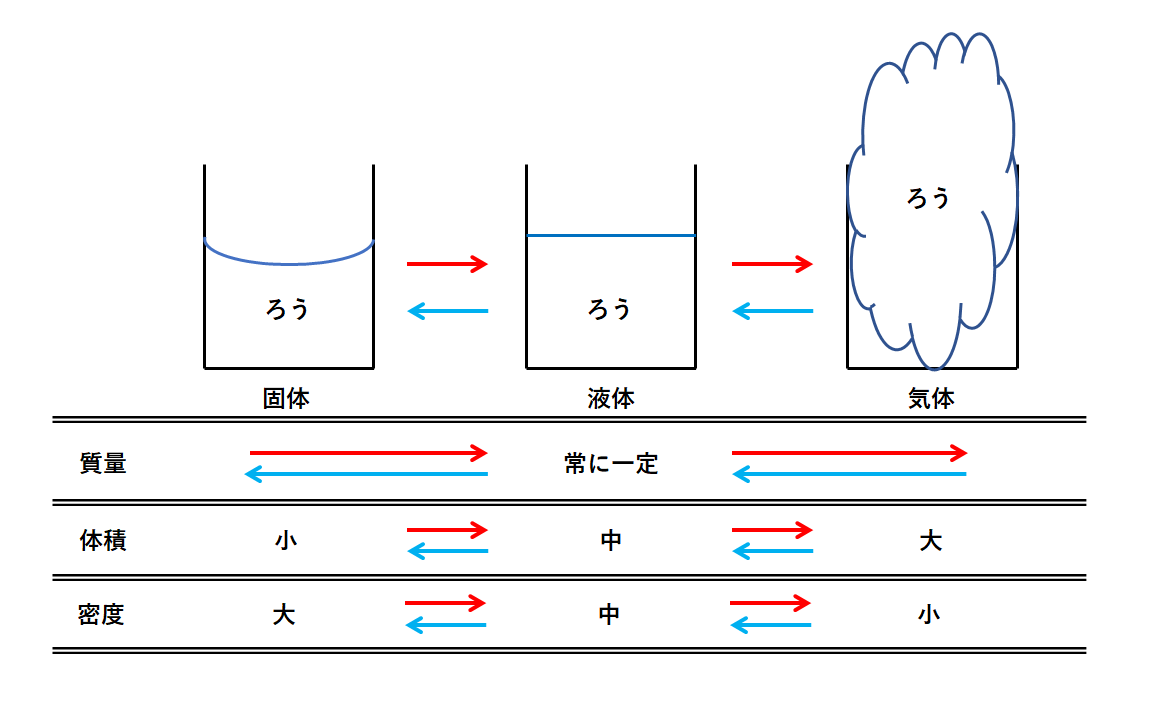
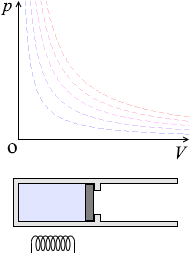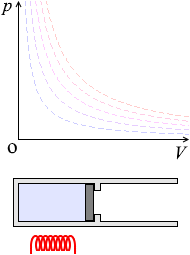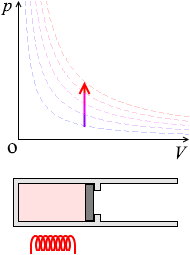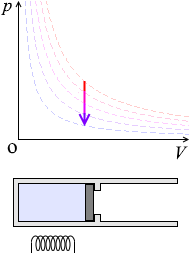
体積が一定のまま、温度や圧力が変化する状態変化を 定積変化 * といいます。 これはピストンを固定しながらシリンダーを加熱、冷却するような状態変化です。 V が一定なので、 W = pΔV の ΔV が 0 であり、つまり W =0 であり、①式 ΔU = Q W は ΔU = Q となります。 ピストンが動かないということは仕事が 0 ということであり、気体に加えられた熱は全て内部エネルギー(=分子のスピー. 気体の性質 気体の種類による特性を見いだすとともに、気体を発生させる方法や捕集法を学ぶ。 状態変化 状態変化によって物質の体積は変わるが質量は変化しないこと、物質は融点や沸点を境に状態が変化することを学ぶ。 物質を分ける 物質が水に溶けるとき水溶液の中では溶質が均一に分散していること、水溶液から溶質を取り出し、溶解度との関連を学ぶ。 物質と原子・分子. 気体の体積変化と仕事 • 気体が体積変化するときの仕事の大きさ • 気体が外からされた(自分が受けた)仕事 を正とする規約 • ΔV=(おわりのV)-(はじめのV) • 符号 圧縮:仕事をされた:δW>0,ΔV<0 膨張:仕事をした:δW<0,ΔV>0.
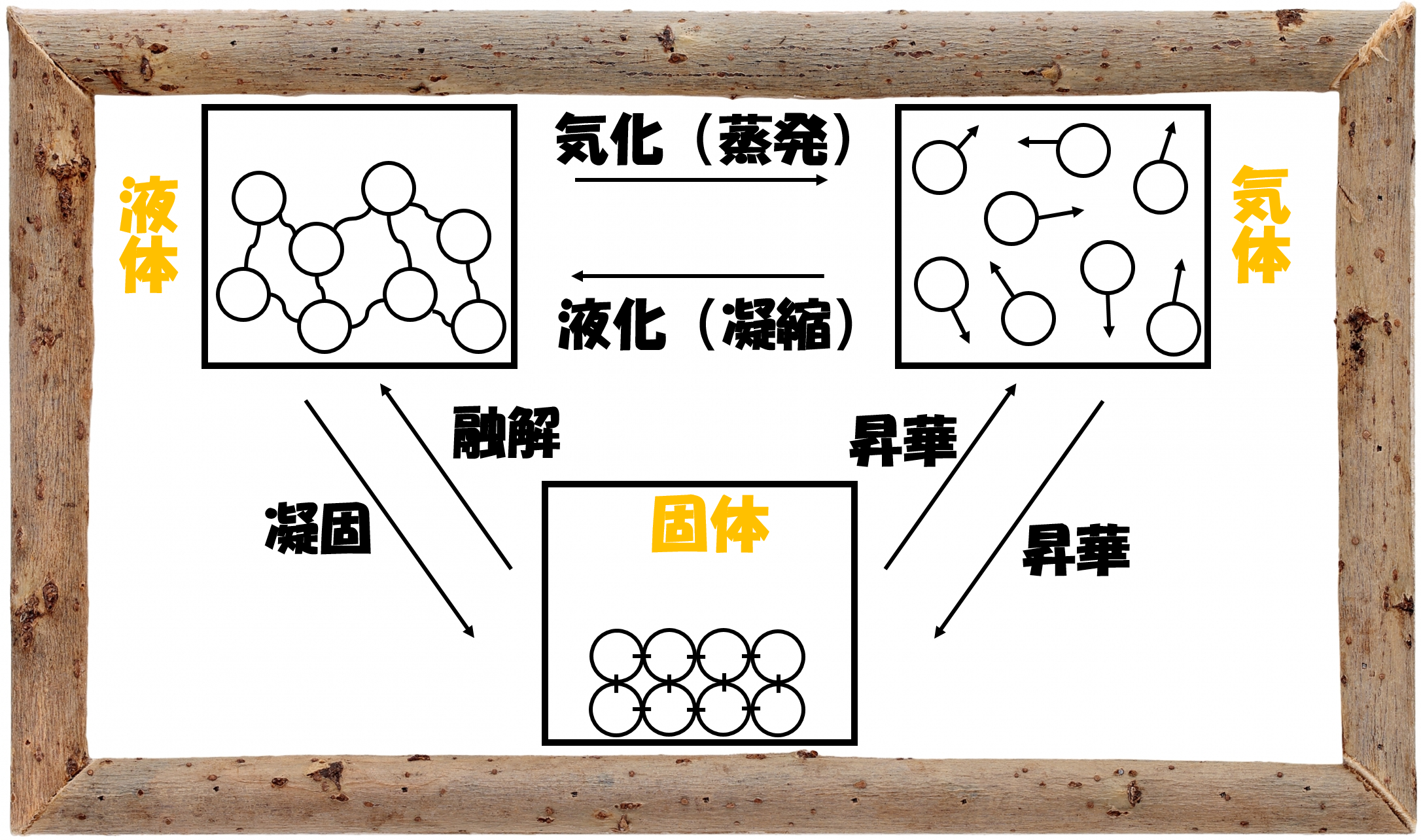
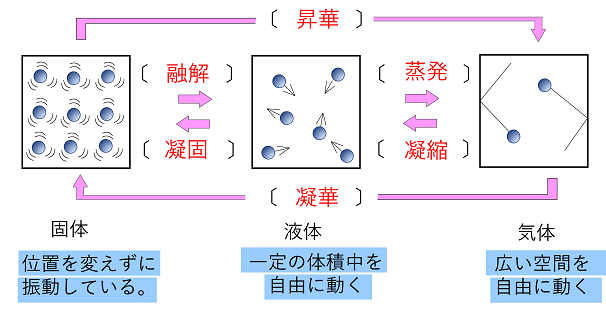
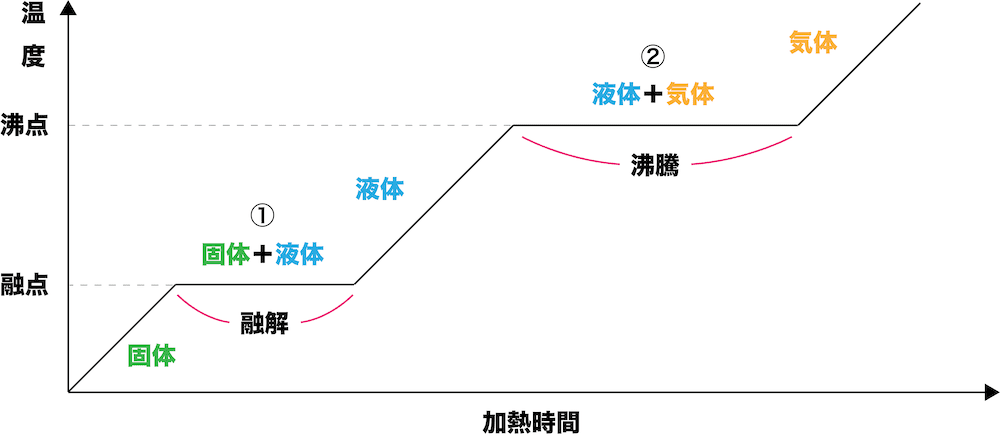
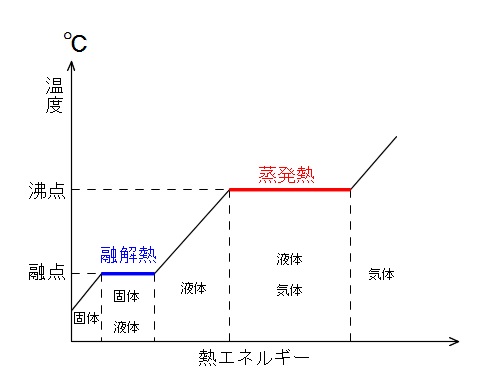
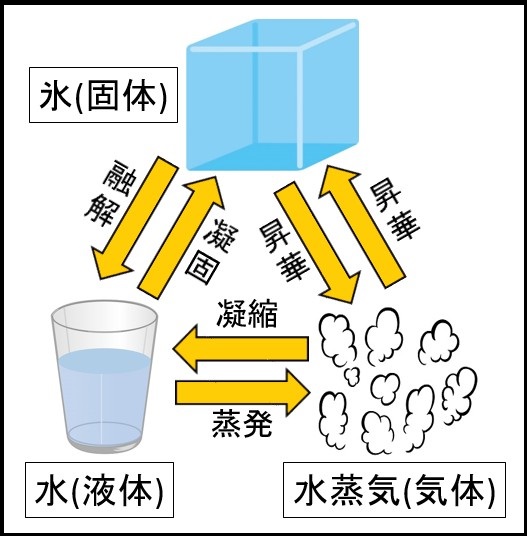
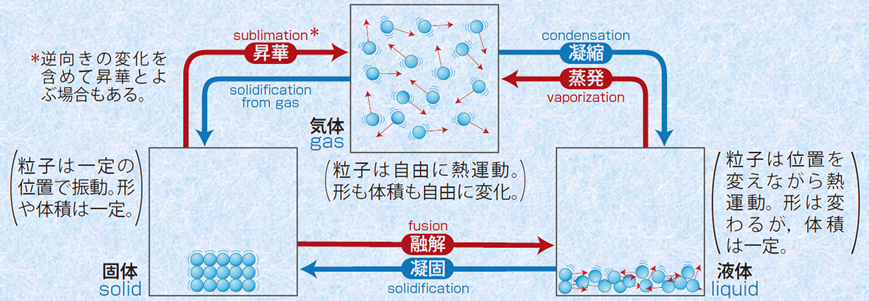
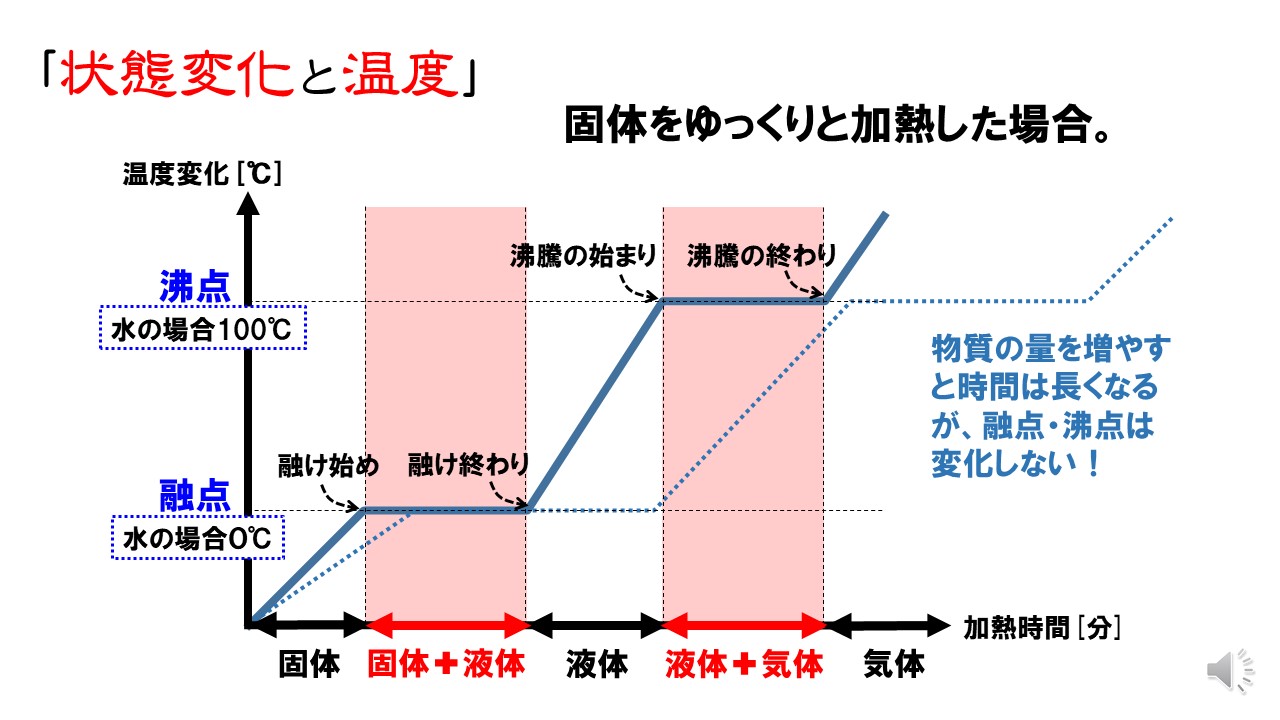
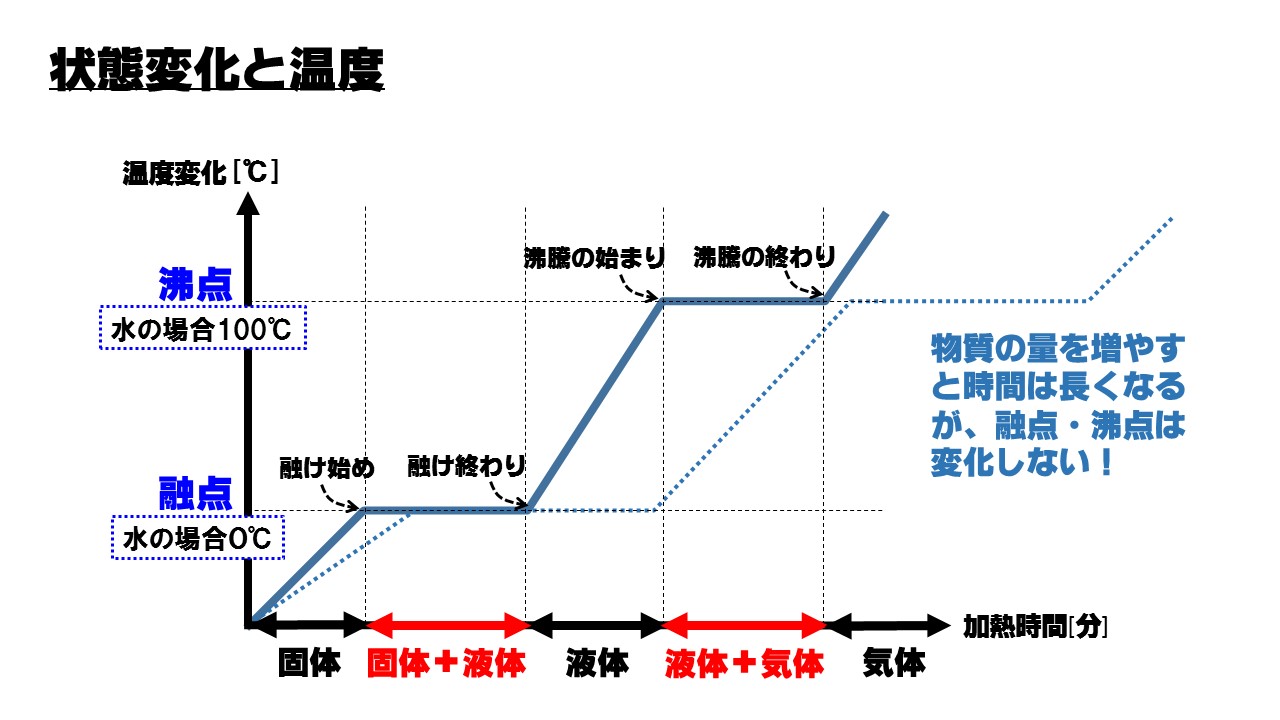
気体は、液体が蒸発するor一部の固体が“昇華”することで生まれる状態です。 非常に各分子の運動が激しく、ファンデルワールス力はほとんど働きません。 固体から気体への状態変化の図 ここからは、より具体的に《固体が、→液体を経て→気体へと変化する》際の『加えた熱量』と『温度の関係』を表したグラフを見ていきます。 <図1>の読み取り方 よく問題集や教科書で見. 気体の状態を,とくに高圧または凝縮温度付近まで精度よく表すために用いられる状態式の一つで,気体の圧力およびモル体積をそれぞれ P , V としたとき,モル体積 V の逆数の冪級数(べききゅうすう: power series )に展開するビリアル展開( virial expansion )で表した方程式。 PV = nRT(1+B/V+C/V2+・・・) B,C,・・・は,それぞれ第二ビリアル係数,第三ビリアル係数. それでは,状態変化からはじめましょう。 気体から液体に変わる変化を凝縮,液体から固体に変わる変化を凝固といいます。 逆に,固体から液体に変わる変化を融解,液体から気体に変わる変化を蒸発といいます。 また,固体から直接気体になる変化を昇華といいます。 気体から固体になる変化も昇華ということがあります。 (1)状態変化 物質がとる固体,液体,気体→物質の三態 気体 液体 固体.
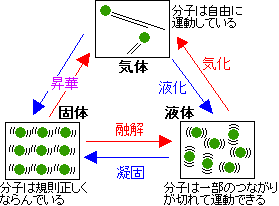
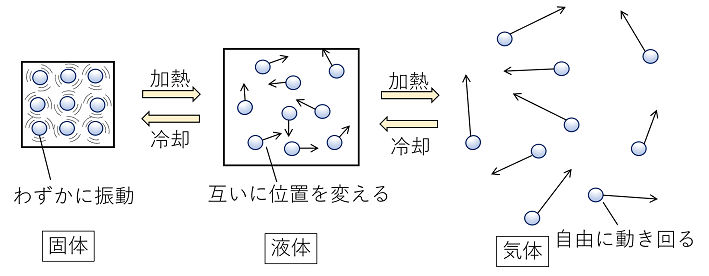
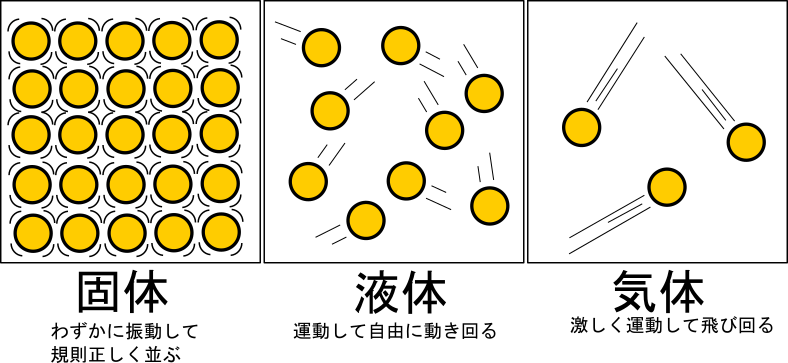
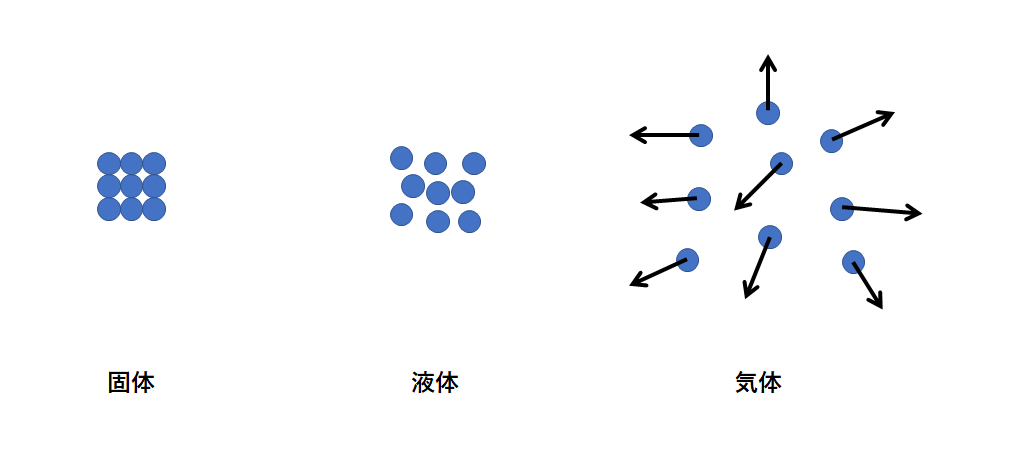
物質は圧力や温度の変化で、 固体 、 液体 、 気体 と状態が変わるのですが、この3つの状態を「物質の三態」といいます。 これは分子や粒子のもつエネルギーで自由度が変わり、集合状態が変わって来るからです。 固体 粒子の熱運動は穏やかで互いにくっつきあっていて、規則正しくならんでいます。 粒子は動き回れる程ではありませんが 振動している 状態です。 氷の粒子である水が動いているよ. 一方、水の表面では、液体から気体への状態変化、「蒸発」が起きている。 温度が ほぼ100℃ になると、水の中から水蒸気の泡が盛んに出てきた。. 断熱自由は準静的な過程ではないので理想気体の状態方程式が変化の過程で成立しない したがって, ポアソンの関係式は成立しない 断熱自由膨張では系が仕事をせず( \( d W =0 \) ), 吸熱/放熱量もゼロ( \( d Q = 0 \) )であるので, 熱力学第1法則より系の内部.
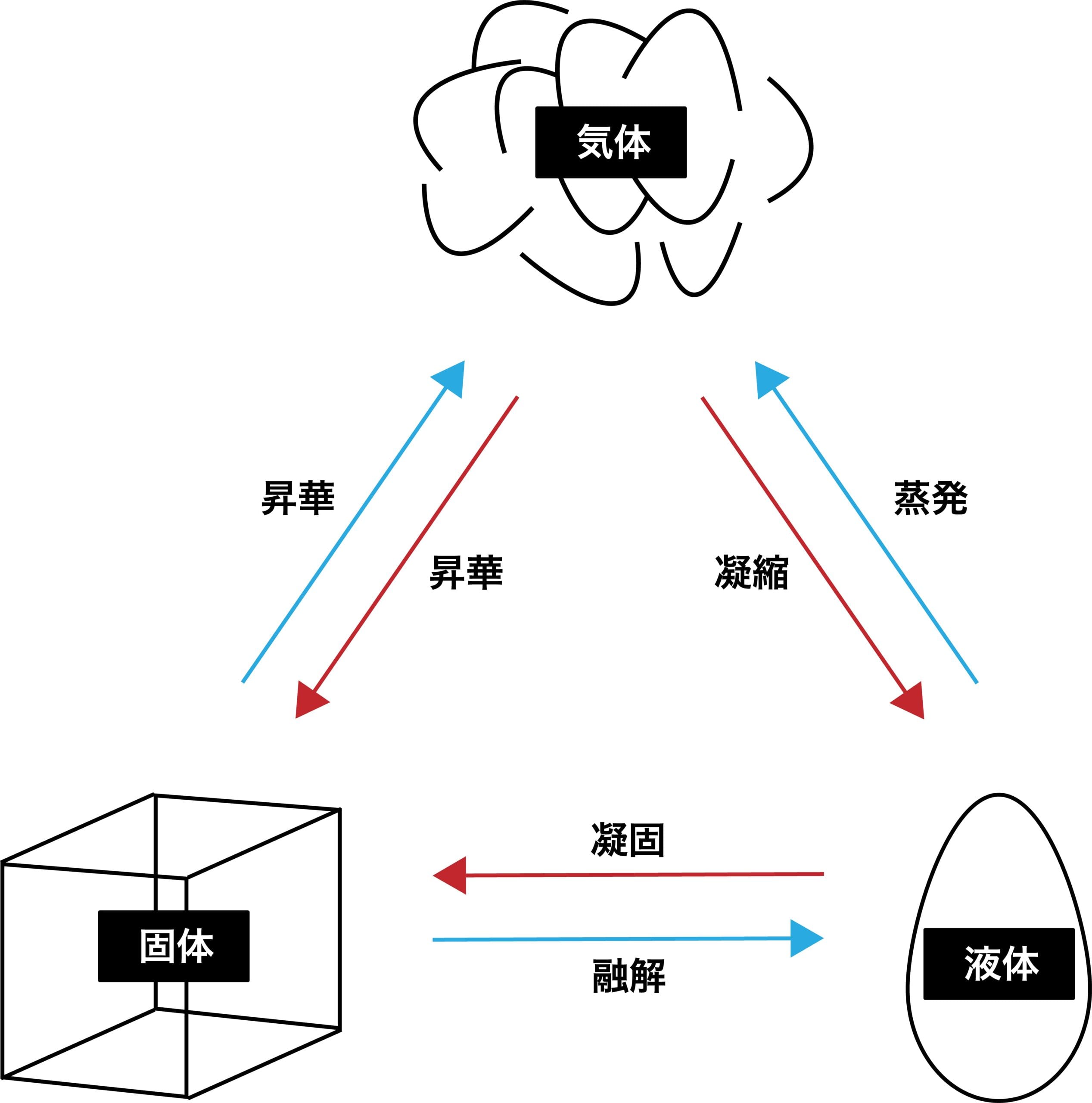
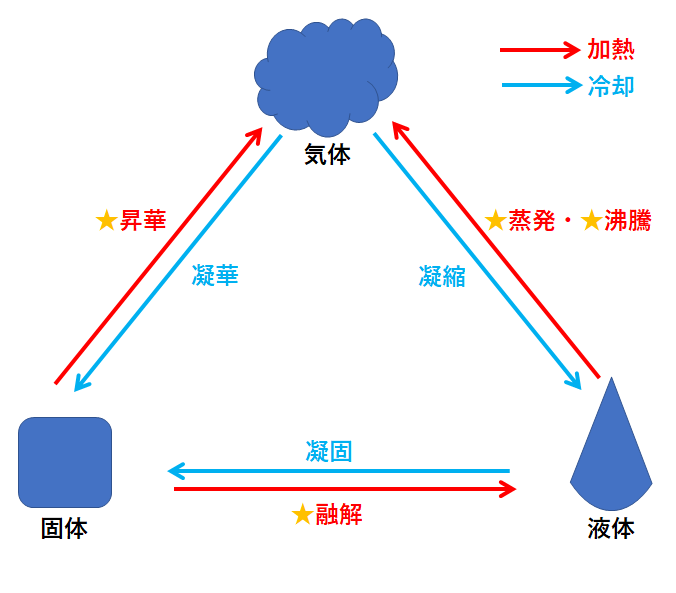
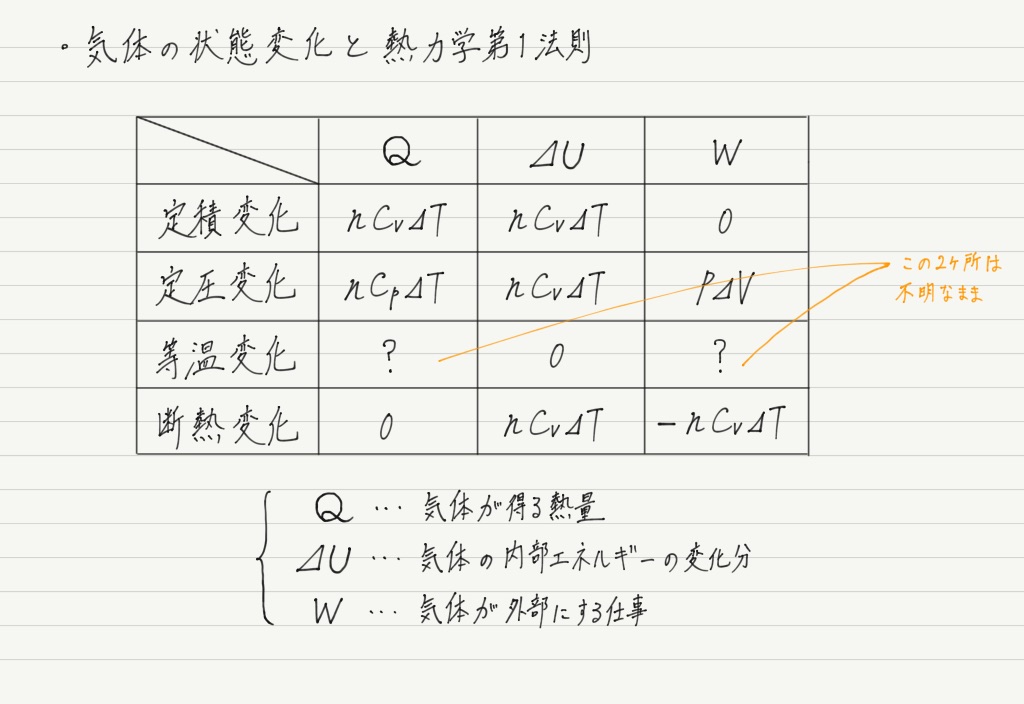
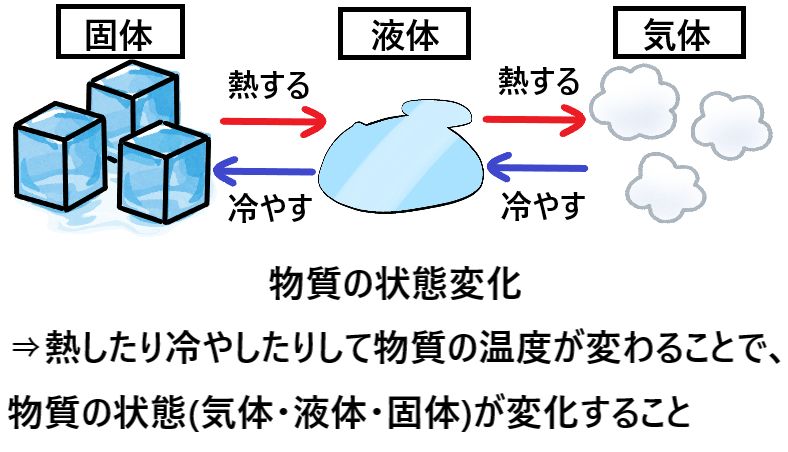
冷却による状態変化 次に、冷却によって熱運動が小さくなり、分子が束縛される変化です。 気体→液体への変化を 「凝縮」 と呼びます。 体積が急激に「縮」んでしまうと覚えましょう。 液体→固体への変化を 「凝固」 と呼びます。 「固」体になって「固」まる変化です。 気体→固体への変化を 「昇華」 と呼びます。 2ランクダウンも、同じく「華」やかなので同じ名前がついていま. 状態変化といえば「固体⇄液体⇄気体」というイメージがありますが、気体の状態へんかは気体の「体積・圧力・温度」の変化のこと。 気体の状態変化は以下の4つを考えましょう。 定積変化:体積が一定 定圧変化:圧力が一定 等温変化:温度が一定 断熱変化:熱の出入りなし 熱力学第一法則より、ΔU = Q W Q:外部から加えた熱量, J W:外部からの仕事, J ΔU:内部エネルギーの. 温度によって物質の状態(固体・液体・気体)が変化すること を言います。 そして 固体・液体・気体の物質の3つの状態のことを”物質の三態”と呼びます 。 上図のように物質には固体・液体・気体の3つの状態が存在していますが、 それらの状態はその物質の温度によって変化します。 例えば水を0℃まで冷やすと少しずつ氷始めたり、 反対に水を熱して100℃に達すると沸騰して水蒸気に変化しま.
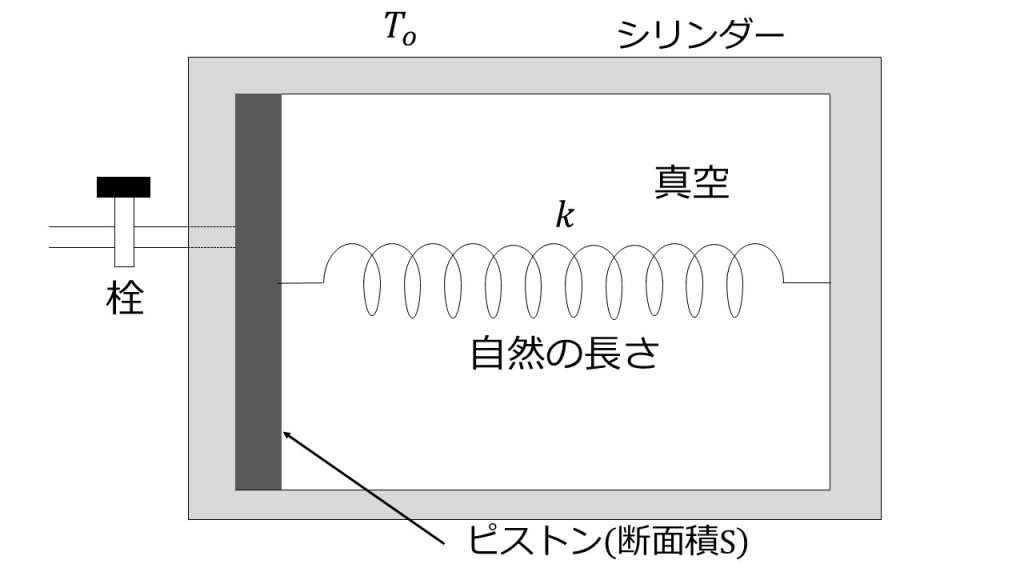
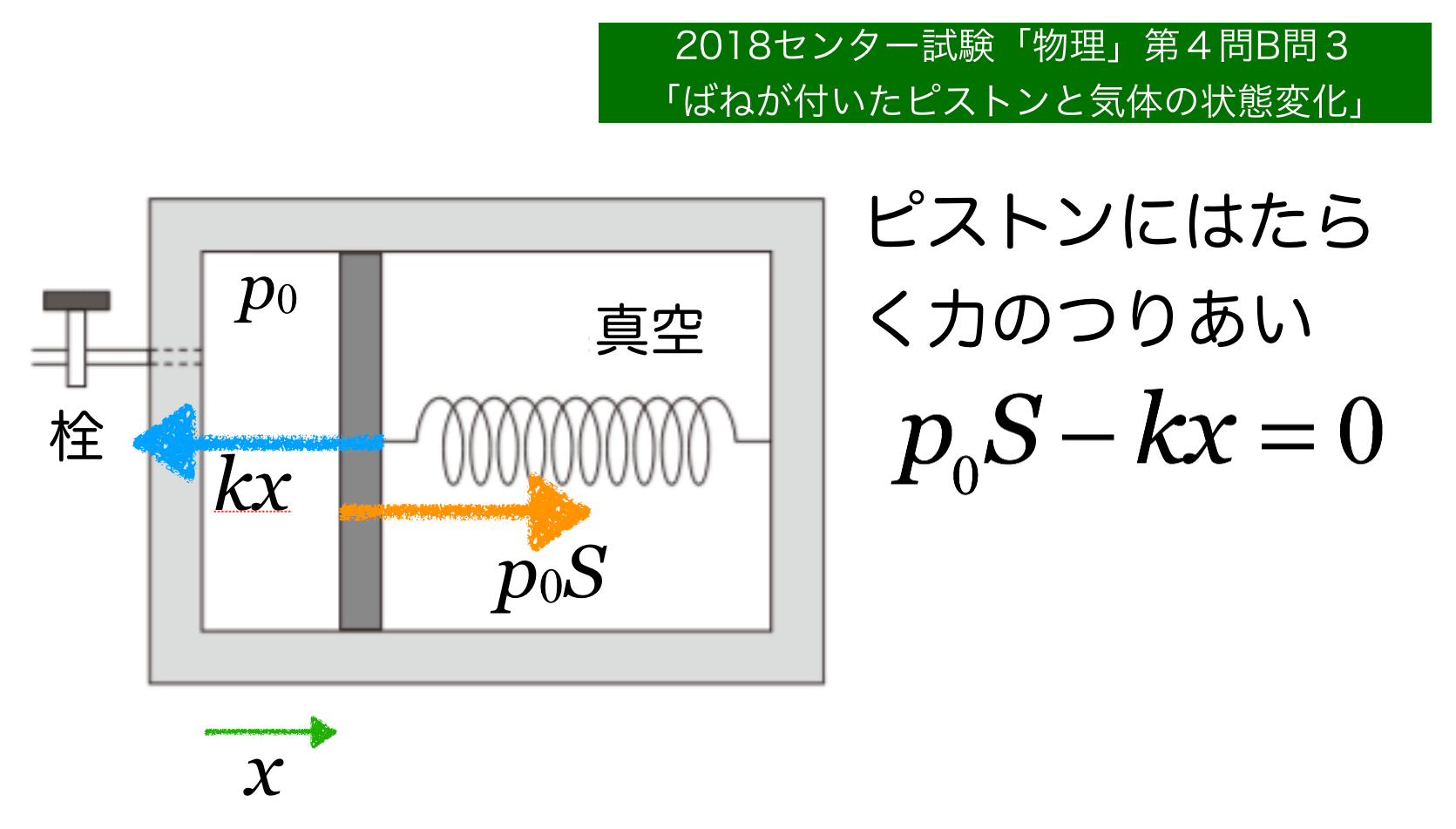
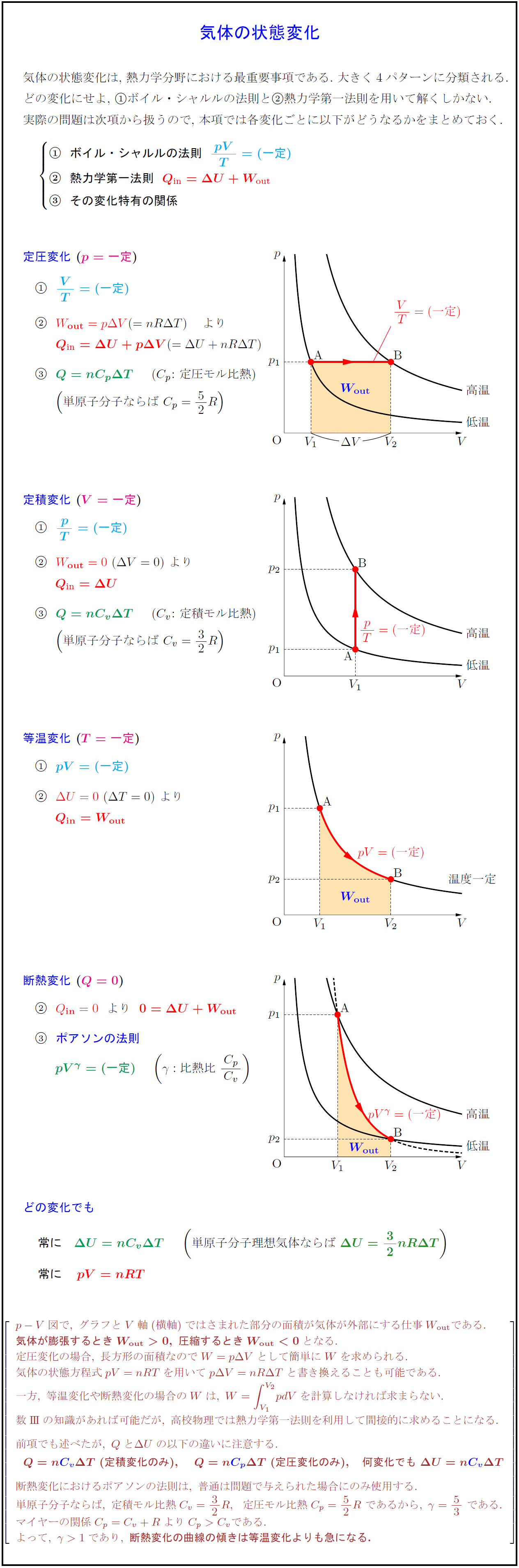
気体の状態変化の解法 ⓪ 力学的な装置を伴うときは,ピストンについて力の間の関係式を立てる。(つり合っているときは「力のつり合い」の式,もしくは,加速度運動しているときは,「運動方程式」) ① (理想気体の)状態方程式(pV=nRT)を立てる。. 例えば水には氷という固体の状態、液体の水の状態、水蒸気という気体の状態があるね。 どんな物質にもこのように三態が存在するよ。 ケミ太 三態の間で、物質の状態が変化するんですね。 博士 それを状態変化というよ。 物質は温度や圧力の条件によって三態の間で状態変化をする んだ。 固体から液体へ状態変化することを融解、液体から気体に状態変化することを蒸発、といった具合に、状態. ※ボイル・シャルルの法則について詳しくは ボイル・シャルル・ボイルシャルルの法則(条件・公式・計算問題の解き方など) を参照 問2 10×10 5 Paで体積が30Lの気体.
気体の状態変化に関する問題です。 以下の問題なのですが解き方が分かりません。 回答お願いできませんでしょうか? 問題1:気体の状態変化について、以下の問に答えよ。 1 物質量1 mol の気体に対して,次の性質を満たすような2 種類の気体を考える.. 状態変化とは? 状態変化とは、 物質が固体から液体に変化したり、液体から気体に変化したりすることを指す言葉 です。 身近なものの例で言えば、水(h 2 o)が「氷(固体)・水(液体)・水蒸気(気体)」と温度の変化によって姿を変えるのがまさにそうですね。 そして、 固体・液体・気体の. 熱力学の原理を利用する機械では、作動物質として気体を扱うものが数多くあります。 気体の状態変化について理解することは、熱力学を学ぶ上で非常に重要です。 1.理想気体 気体の状態変化を論ずる上では先ず、気体分子間の相互作用のない仮想的な状態である理想気体に関する法則が.
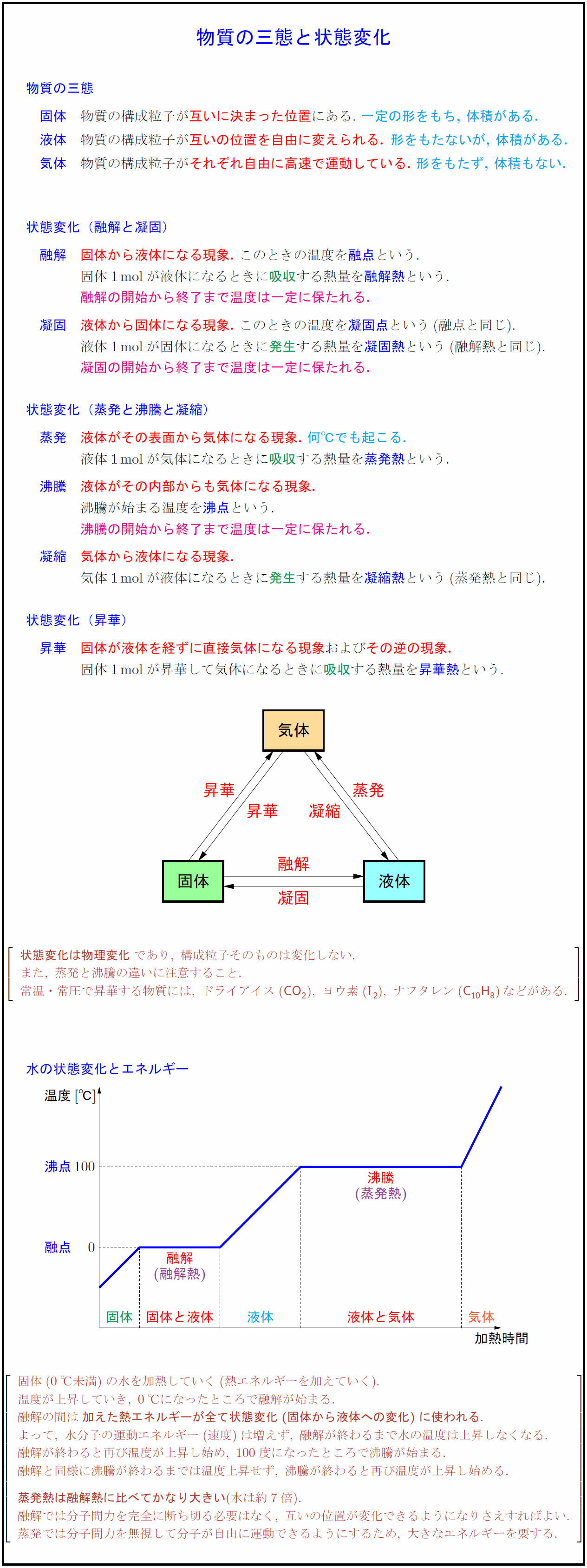
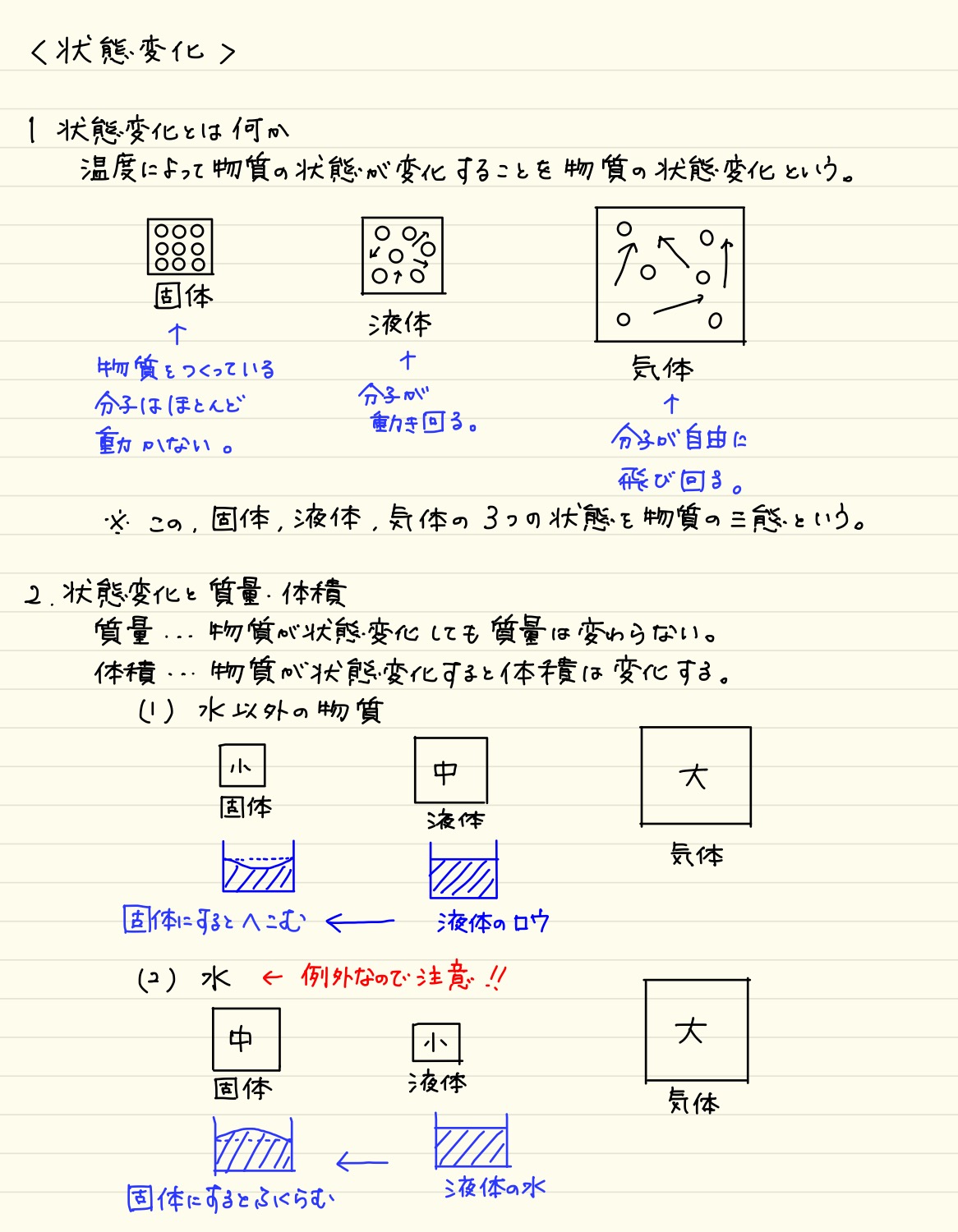
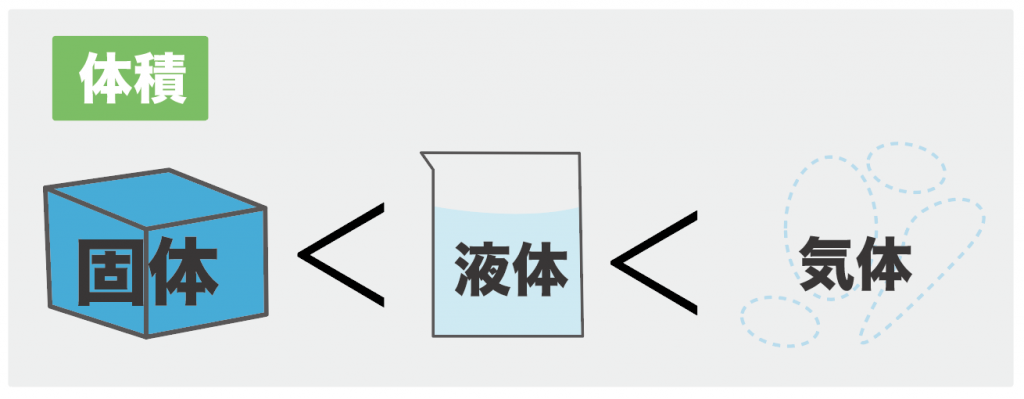
気体のエタノール(アルコール)の体積の求め方 まず、標準状態では気体はどのような物質であっても、1molあたりその体積は224Lとなります。 かつ、エタノールの化学式は上述のようC2H5OHで表されることからその分子量は「12×2 1×6 16=46g/mol」と変換でき. 気体の状態変化とは,気体の系において 圧力,体積,温度 が変化することを表します。 特に高校物理においては,熱力学第一法則とボイル・シャルルの法則を利用して,気体の状態がどのように変わるかを考察します。 なお,気体が外部から吸収した熱量を Q Q , Q Q による内部エネルギー変化を \Delta {U} ΔU ,気体が外部にした仕事を W W として, 熱力学第一法則 Q=\Delta. 物質は、温度や圧力の変化によって固体、液体、気体の3つ状態に変化します。 これを物質の三態(ぶっしつ の さんたい)といいます。 ちなみに、消防法で規制されている危険物には固体と液体はありますが、気体のものはありません。 物質の状態変化は、火災の消火活動にも密接に関わっています。 危険物と関連づけながら確認していきましょう。 融解と凝固 蒸発と凝縮 沸騰と沸点 昇華 融解と凝.
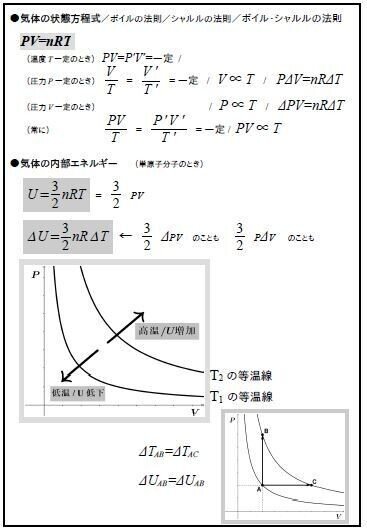
物質の状態についてどの程度ご存じでしょうか。私たちは、 固体 ・ 液体 ・ 気体 の3つの状態があることは分かると思います。 しかし、前記の三態の変化、エネルギーに関しての細かな内容は難しい内容であり分からないという方も多いと思います。. 2 物質の三態と状態変化 k 状態変化 物質は〔 温度 〕,〔 圧力 〕によって〔 固体 〕,〔 液体 〕,〔 気体 〕と状態を変化させる。 この物質がとりうる 3 つの状態を物質の三態という。 蒸発はどんな温度でも起こる。沸騰はある一定の温度になると起こる。. 気体の状態変化の問題では,\ 基本的には次を用いて解くことになる { ボイル・シャルルの法則\ {pV}{T}=(一定) 熱力学第一法則\ Q_in=Δ UW_out その変化特有の関係 各変化ごとに,\ 結局これらがどのような式になるかをおさえておけばよい pV図で,\ グラフとV軸(横軸.
理想気体(完全気体)の状態方程式:pV=nRT を用いる事によって、 d'w=pdV=nRT/p dp である事が分かります。両辺を積分して、 w=∫d'w=nRT∫(1/p)dp よりwが求まります。(Tは定数(等温変化)なので、積分の外に出しました).
気体の状態変化 断熱変化 熱効率 物理
例題 理想気体の性質と状態変化 6 等温変化 数学活用大事典

物質の状態変化 要点まとめ 気体 液体 個体 融点 沸点 中学理科 Yattoke 小 中学生の学習サイト
気体 の 状態 変化 のギャラリー

物質の三態変化を慶應生が図で超絶わかりやすく解説してみた 高校生向け受験応援メディア 受験のミカタ
状態変化と圧力 体積 ねこでもわかる化学
1
物質の三態と熱量の計算方法をわかりやすいグラフで解説
中1化学 状態変化 中学理科 ポイントまとめと整理

熱力学 12 定圧変化と等温変化の違い 理系への道

断熱変化 高校物理 熱力学 気体の状態変化 断熱変化 単原子分子理想気体の場合 授業 Youtube
物質の状態変化

物質の三態と状態変化 乙4特訓
中学受験の理科 氷 水 水蒸気 状態 固体 液体 気体 の変化 中学受験 理科 偏差値アップの勉強法

小テスト 気体の状態変化 その1 物理教育の現場から
物質の三態 状態変化とは 原理や用語 凝縮 昇華等 を図を使って解説 化学のグルメ
気体の状態変化 断熱変化 熱効率 物理

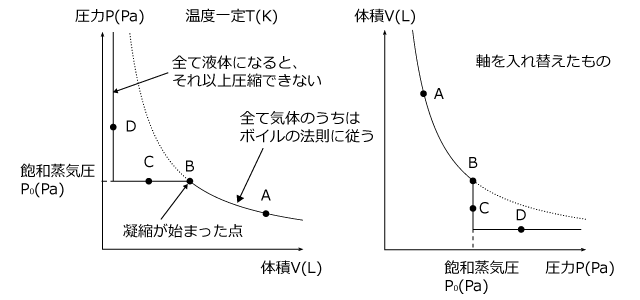
化学 実在気体の状態変化について 真ん中のグラフについての質問です Clearnote

物質の状態変化 無料で使える中学学習プリント
中1化学 状態変化 中学理科 ポイントまとめと整理

高校物理 理想気体の状態方程式 Pv Nrt 受験の月

定圧比熱と定積比熱 熱力学の第一法則4 色と形で気象予報士

気体の状態変化 熱 センター物理対策過去問題集
中1理科 状態変化 質量 体積 密度の変化 Pikuu
化学講座 第40回 実在気体のp V P Tグラフ 私立 国公立大学医学部に入ろう ドットコム

Web教材イラスト図版工房 R C1m 固体 液体 気体の状態変化と体積 1
3
物質の三態と熱運動

熱機関 理想気体の状態変化 物理基礎 気体の法則と気体の状態変化 Hamako Ssh
等温変化 仕事

物理ネコ教室4気体の状態変化 ひろじの物理ブログ ミオくんとなんでも科学探究隊

気体の状態変化とモル比熱 断熱変化 等温変化 定圧変化など 高校生から味わう理論物理入門
高校物理 気体の状態変化 まとめ Blastopore Note
状態変化のまとめ 高校物理をあきらめる前に 高校物理をあきらめる前に

高校物理 気体の状態変化 Youtube

この解き方が全くわかりません 簡単にわかる方法を教えてください Clearnote
中1化学 状態変化 中学理科 ポイントまとめと整理

8 気体の状態変化 物理解説 効率的スキルアップ術

スタディピア 物質の状態変化
気体の状態変化なんですけど 写真の一周ってところがわかりません おしえ Yahoo 知恵袋

なぜ融点や沸点は物質によって違うのか

中1理科 3分でわかる 状態変化とは一体何もの Qikeru 学びを楽しくわかりやすく
状態図とは 見方 例 水 鉄 理系ラボ

等温 定圧 定積変化とp Vグラフ 高校物理の備忘録
気体の状態変化 わかりやすい高校物理の部屋

スタディピア 物質の状態変化
ファン デル ワールスの状態方程式 クラウジウス クラペイロンの式 ジュール トムソン効果

理想気体の状態変化 物理学の気体の状態変化についてです 以下 問題文 Okwave

機械設計マスターへの道 気体の状態変化 熱力学の基礎知識 アイアール技術者教育研究所 製造業エンジニア 研究開発者のための研修 教育ソリューション
気体の状態変化 わかりやすい高校物理の部屋
物質の三態 状態変化とは 原理や用語 凝縮 昇華等 を図を使って解説 化学のグルメ

高校物理 熱力学 動画で学べるリンク集 家庭学習用プリント学年別リンク集
化学講座 第31回 熱化学方程式 状態変化と熱の出入り 私立 国公立大学医学部に入ろう ドットコム

状態変化
物質の状態変化とエネルギー 物質の三態と状態図
物質の三態と状態変化
化学の実在気体の状態変化のグラフで 上のグラフは圧力が上がって飽和蒸 Yahoo 知恵袋
Web教材 Naclの状態変化 水への溶解 Ver 1 12 09 9 7
状態変化とは何か 物質が状態変化する仕組みを簡単に図解
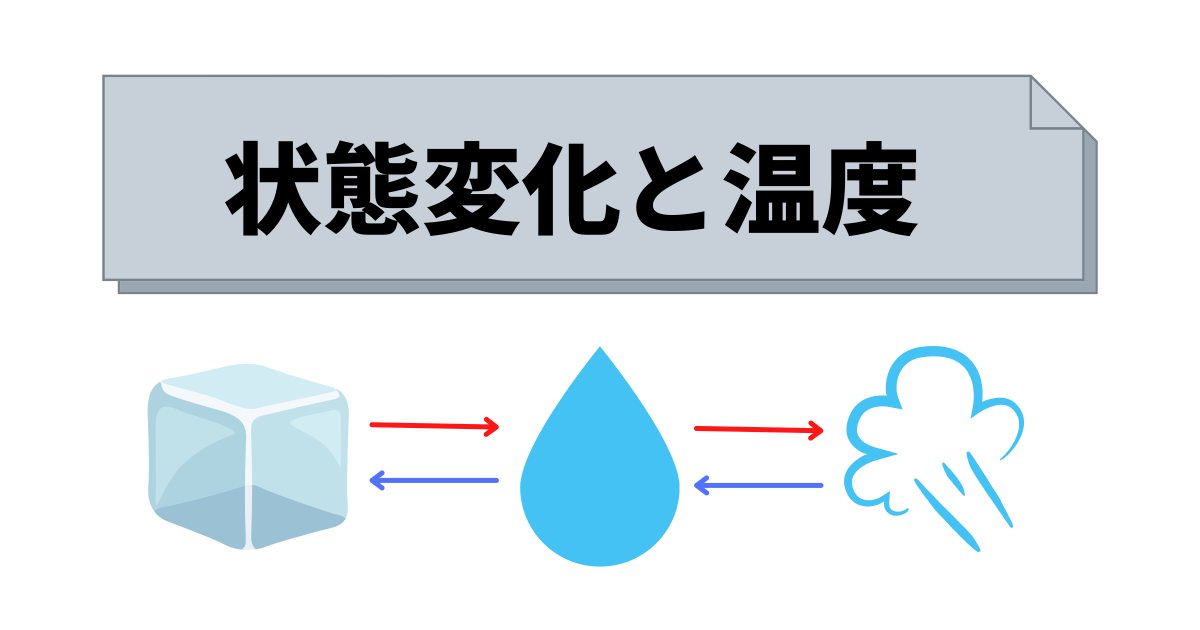
温度による状態変化と身近な例 中学理科 Hiromaru Note

ม 1 โน ตของ 物質の状態変化 液体 気体の変化 ช น Clearnote

高等学校化学ii 物質の三態 Wikibooks
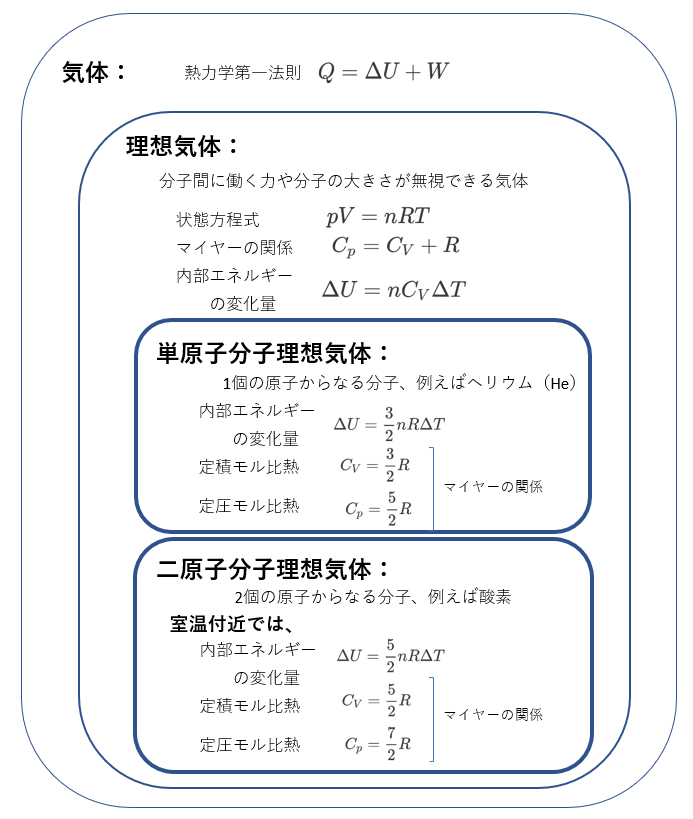
P Vグラフ
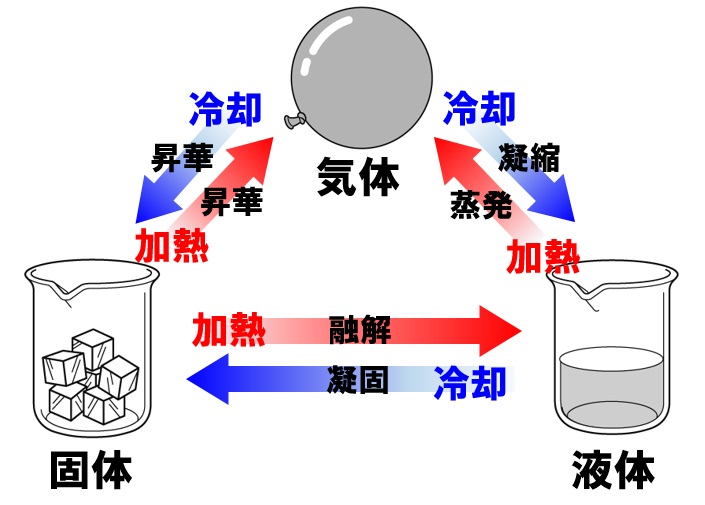
中1理科 状態変化と質量 体積 密度のポイント Examee

気体の状態方程式とは 体積との関係から練習問題まで 高校生向け受験応援メディア 受験のミカタ
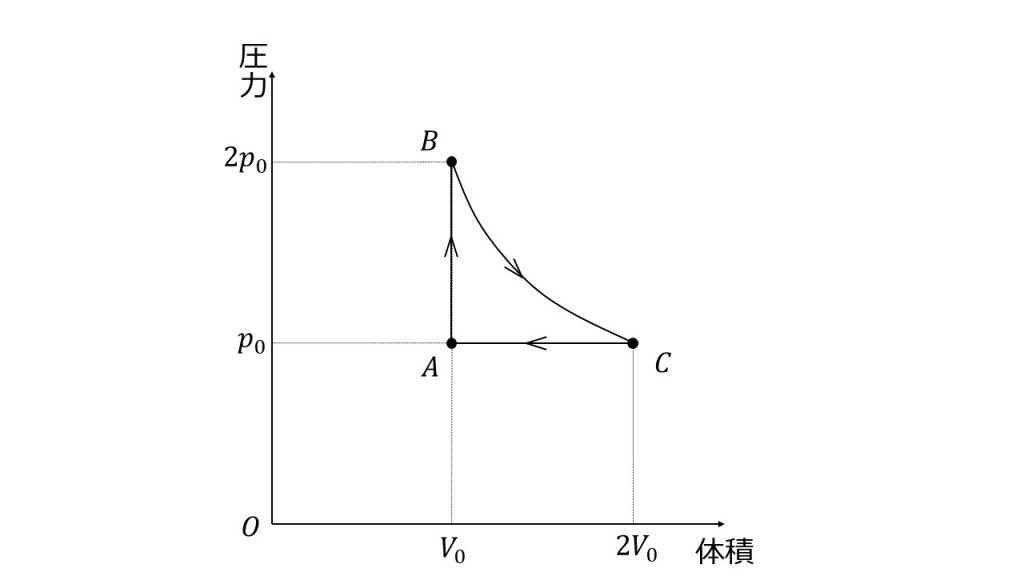
気体の状態変化 熱力学 問題演習 17年センター試験本試物理第3問b 大学受験の王道

第93章 理想気体の状態方程式
気体の状態変化とモル比熱 断熱変化 等温変化 定圧変化など 高校生から味わう理論物理入門

物質の三態と状態変化

理想気体 状態方程式 高校物理 熱力学 気体の状態変化2 状態方程式 授業 Youtube

気体 液体 固体の間での状態変化と熱の出入り 密度や体積の関係を解説

高校物理 気体の仕事 P Vグラフの面積 練習編 映像授業のtry It トライイット
状態変化とは何か 物質が状態変化する仕組みを簡単に図解

気体の状態変化 でわからない問題があります 1molの単原子分子理想 物理学 教えて Goo

固体 液体 気体 状態変化で体積 密度はどのように変わる 中学数学 理科の学習まとめサイト

物理 気体の状態変化 高校生 物理のノート Clearnote

高校物理 それぞれの特徴を捉えよう 気体の状態変化 熱力学 お茶処やまと屋

熱力学 11 等温変化 理系への道
物質の状態変化とは 水での例や融点 沸点と一緒に徹底解説 とはとは Net
気体の状態変化 熱力学 問題演習 18年センター試験本試物理第4問b 大学受験の王道

気体の状態変化ってなに わかりやすく解説 受験物理ラボ
状態変化
高校理論化学 物質の三態 固体 液体 気体 水の状態変化とエネルギー 受験の月

物質の三態変化 融解 凝固 蒸発 凝縮 昇華 と状態図 The Calcium

物質の状態 Wikipedia

等温 定圧 定積変化とp Vグラフ 高校物理の備忘録
センター18物理第4問b ばねが付いたピストンと気体の状態変化 理科が好き Com
中1理科 状態変化 温度の変化 Pikuu
固体 液体 気体の違いは運動の違い 理科の授業をふりかえる

理科とか苦手で 状態変化1 状態変化と熱 1 状態変化とは
3

物質の状態 固体 液体 気体 の達人

大学入試演習 熱力学4 気体の状態変化 お茶処やまと屋

気体の状態変化 シリンダー ばね 気体の状態変化についての問題で 物理学 教えて Goo

理想気体の状態変化 汚泥乾燥機 スラリー乾燥機 ヒートポンプ汚泥乾燥機 Kenki Dryer

等温 定圧 定積変化とp Vグラフ 高校物理の備忘録
中1化学 状態変化 中学理科 ポイントまとめと整理
温度による状態変化と身近な例 中学理科 Hiromaru Note
高校物理 気体の状態変化 定圧変化 定積変化 等温変化 断熱変化 受験の月
中1理科 状態変化と温度変化のポイント Examee
P Vグラフと気体のする仕事 高校物理をあきらめる前に 高校物理をあきらめる前に

第96章 理想気体と実在気体
状態変化 塾の質問箱
中1理科 3分でわかる 状態変化とは一体何もの Qikeru 学びを楽しくわかりやすく

熱力学 理想気体の状態方程式 状態変化のサイクル2 Pv nrt 高校物理熱力学の第一法則 定積変化等温変化定圧変化 熱効率 気体が取り入れた熱量 気体が放出した熱量 気体が外部にした仕事 Youtube




